Criptosporidiosis en terneras: el secreto está en el ciclo II
DICIEMBRE 2024 | RECRÍA
¿CUÁLES SON LOS PRINCIPALES FACTORES
DE RIESGO EN UNA GRANJA DE LECHE?
Los factores de riesgo más importantes giran en torno al ciclo del parásito y a la contaminación del ambiente. De ahí que, uno de los principales factores de riesgo para que un ternero se infecte por C. parvum, es estar en contacto con otro ternero que sufra una diarrea por criptosporidios, debido a la alta eliminación de ooquistes y a la baja dosis infectante. Un escenario similar sucede cuando se aloja un ternero recién nacido en una caseta en la que el ternero anterior padeció diarrea. Esto explica por qué el riesgo de criptosporidiosis se incrementa en los rebaños de mayor tamaño en producción intensiva (Brainard et al., 2020), ya que, a mayor cantidad de nacimientos, aumenta la probabilidad de que algún ternero, entre 7 y 20 días de vida, excrete ooquistes y, por tanto, también el riesgo de contagiar a algún ternero en su primera semana de vida, cuando son más susceptibles a la infección. No obstante, también las granjas de menor tamaño se ven frecuentemente afectadas, dado que el manejo tradicional, con menores estrategias de limpieza y contacto entre animales de distintas edades, también puede favorecer la presencia del parásito (Castro-Hermida, 2002).
Asimismo, un punto a tomar en cuenta para el diagnóstico y el control es que un porcentaje de los terneros sin diarrea también pueden eliminar C. parvum en las heces (Díaz et al., 2021), siendo otra potencial fuente de infección.
Por otro lado, no está tan claro cuál es el papel de las vacas adultas y el riesgo de transmisión de C. parvum de madre a ternero. La ciencia ha demostrado que un porcentaje de las vacas adultas eliminan C. parvum en las heces (Díaz et al., 2021; Shaw et al., 2021). Sin embargo, no hay evidencias concluyentes de que se incremente el riesgo de presentar criptosporidiosis al nacer en una paridera común o dejar al ternero con la madre un tiempo (Trotz-Williams et al., 2008). Aun así, que la evidencia científica sea limitada, no descarta que sea un posible origen de contagio.
¿PUEDO ELIMINAR A CRYPTOSPORIDIUM PARVUM DE MI GRANJA?
Pues, una vez presente la infección en los terneros, parece una tarea complicada, teniendo en cuenta que los ooquistes pueden sobrevivir largos periodos de tiempo en ambientes húmedos y que son resistentes a la mayoría de los desinfectantes. Por ello, aunque no se puedan eliminar de la granja, es fundamental minimizar la presión de infección con la que tiene que convivir el ternero, ya que, cuanto mayor es la cantidad de ooquistes ingeridos de C. parvum, mayor es el porcentaje de terneros con diarrea y antes se inicia la enfermedad y la excreción de ooquistes (Zambriski et al., 2013).
Teniendo en cuenta que la infección es vía fecal-oral, y que la susceptibilidad de los terneros decrece con la edad, los siguientes puntos de manejo se consideran claves para minimizar la presión de infección en las primeras semanas de vida (imagen 3):
- Limpieza con agua y una solución de alcalino clorado de los utensilios de alimentación (Trotz- Williams et al., 2008).
- Limpieza y desinfección de los alojamientos. Los suelos de cemento parecen disminuir el riesgo en comparación con otras superficies (Brainard et al., 2020)
- El movimiento de terneros en grupos y no de manera individual disminuye el riesgo de trasmisión (Silverlås et al., 2009), así como dejar periodos de vacío sanitario de las instalaciones antes de introducir nuevos terneros.
- Las botas, monos de trabajo, etc. pueden ser potenciales vías de diseminación dentro de un rebaño, de ahí la importancia de la limpieza y el cuidado a la hora de pisar los comederos.
- La contaminación de las fuentes de agua de la granja y la contaminación fecal de los bebederos aparecen como una vía de transmisión de difícil diagnóstico y control.

Imagen 3. Diferentes factores de riesgo potenciales a la hora de infectar un ternero por C. parvum: a) terneros con diarrea, b) paridera, c y d) materiales de alimentación, e) agua y f) botas
Por último, es importante destacar que una limpieza y desinfección inadecuadas pueden favorecer la diseminación de ooquistes dentro de un rebaño (Díaz et al., 2018). Para que sea eficaz, es fundamental realizar una limpieza previa antes de la desinfección, ya que los desinfectantes pierden eficacia en presencia de materia orgánica. Asimismo, se debe tener especial precaución con los sistemas de limpieza con agua a alta presión, ya que, en espacios cerrados, pueden diseminar los ooquistes por la nave a través de los aerosoles que genera.
SI TENEMOS QUE CONVIVIR CON EL PARÁSITO,
¿CÓMO PODEMOS MINIMIZAR SU IMPACTO?
Hasta hace poco tiempo, los tratamientos metafilácticos eran la única opción para el control de la criptosporidiosis. Sin embargo, desde la publicación del Reglamento (UE) 2019/6 del Parlamento Europeo, su prescripción tiene que estar justificada y nunca puede realizarse para compensar una falta de higiene o de medidas preventivas.
Una de las dos alternativas de tratamiento es el lactato de halofuginona. Es un criptosporidiostático que, administrado a partir de las primeras 48 horas durante la primera semana de vida, ha demostrado beneficios en la salud de los terneros, reduciendo la diarrea, la excreción de ooquistes y la mortalidad (Brainard et al., 2021), siempre que se siga correctamente el protocolo de tratamiento (Niine et al., 2018). Por otro lado, la paromomicina, un antibiótico clasificado por la agencia europea del medicamento (EMA) como grupo C, para su uso con cautela, también ha mostrado eficacia en la reducción de la diarrea y la excreción del parasito (Aydogdu et al., 2018). No obstante, su administración debe ser restringida a los casos clínicos que lo requieran, dado que su uso incorrecto puede favorecer la aparición de resistencias bacterianas a los antibióticos.
OPORTUNIDAD DE LA VACUNACIÓN
La vacunación frente a rota-coronacoli ha desempeñado un papel crucial en la prevención de la diarrea neonatal. Sin embargo, hasta hace muy poco no se disponía de una vacuna frente a C. parvum. Afortunadamente, se ha lanzado muy recientemente una innovadora vacuna que permite proteger a los terneros frente a la criptosporidiosis. Esta vacuna, al igual que la de rota-corona-coli, se aplica en las madres durante el último tercio de gestación, incrementando la resistencia inmunitaria de los terneros a través de anticuerpos específicos presentes en el calostro y leche de transición de las madres vacunadas. La protección de los anticuerpos vacunales frente a la glicoproteína Gp40 del parásito en la luz intestinal actúa frente al menos 4 fases del parásito dificultando la infección de las células intestinales y su replicación, y minimizando con ello la gravedad y duración del cuadro clínico (Timmermans et al., 2023). Por eso, continuar dando leche de transición de las madres vacunadas durante los primeros cinco días de vida es vital para aprovechar al máximo la protección de la vacuna.
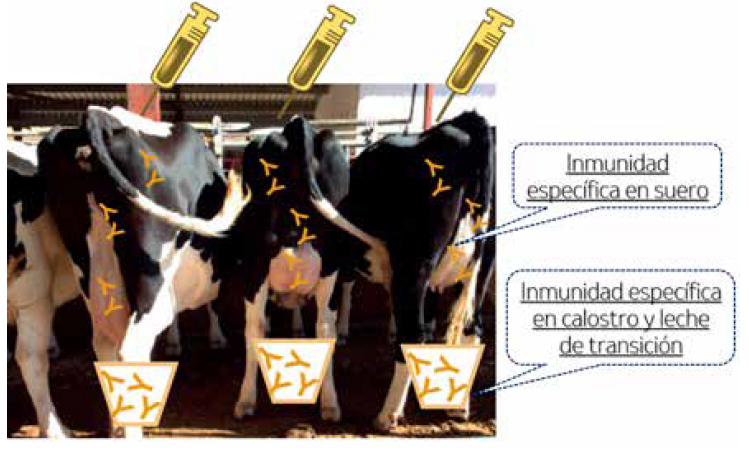
Imagen 4. Vacunando a las madres en el último tercio de gestación podemos transmitir
la protección al ternero a través del calostro y la leche de transición
CONCLUSIONES
Las principales claves del éxito de C. parvum radican en la elevada contaminación que genera, a partir de un único animal infectado, liberando grandes cantidades de ooquistes muy resistentes en el ambiente. A esto se suma su capacidad para infectar a otro ternero recién nacido con una dosis infectante mínima. Además, es destacable la interacción sinérgica de este parásito con otros patógenos entéricos, especialmente víricos, cuya acción inmunosupresora podría facilitar el desarrollo del ciclo interno del protozoo.
Afortunadamente, el ganadero puede controlar la criptosporidiosis mediante un manejo adecuado, la implementación de correctas pautas de limpieza y la oportunidad que surge de la vacunación para maximizar la inmunidad de sus terneros frente a C. parvum. Eso sí, tengan presente que el verdadero secreto del éxito de una ganadería frente a la criptosporidiosis radica en la suma de pequeños esfuerzos repetidos un día sí y otro también.
Autor

Carlos Carbonell

Pablo Díaz
DIAGNÓSTICO | PREVENCIÓN | SALUD | TERNERAS
Artículos relacionados

POR FAVOR, INDICA CUÁL ES TU PROFESIÓN
ARTÍCULOS MÁS LEÍDOS
Cómo se gestiona la recría en Granja Santa Teresa
Nos adentramos en la finca El Gróo
Conoce la importancia de estimar el tiempo del aborto
La importancia de la evaluación reproductiva del toro
Cómo prevenir la diarrea neonatal
CATEGORÍAS
ETIQUETAS
ABORTOS · ANTIBIÓTICOS · BIENESTAR · BVD · CALIDAD · CALOSTRO · COMPOSICIÓN · CORPORAL · CONDICIÓN CORPORAL · CONSEJOS · DATOS · DATOS ECONÓMICOS · DATOS PATOLÓGICOS · DATOS PRODUCTIVOS · DATOS REPRODUCTIVOS · DESAFÍO · DIAGNÓSTICO · ECOGRAFÍA · EFICIENCIA PRODUCTIVA · ENCALOSTRADO · EXTENSIVO · FUTURO · GANADERO · GRANJA · INGLÉS · INMUNOGLOBULINA · LECHE · LENGUA AZUL ·NEUMONÍA · PI · PREINSEMINACIÓN · PREVENCIÓN · RENTABILIDAD · SALUD · SEMEN · SERVICIO · SOSTENIBILIDAD · SRB · TERNERAS · TESTAJE · TESTIMONIO · TOMA DE DECISIONES · TORO · VACUNACIÓN · VACUNO · VETERINARIO · VIRUS · VOCABULARIO



